Welche haben die kürzeren Schwefel-Sauerstoff-Bindungen # SO_3 # oder # SO_3 ^ (2 -) #?
Antworten:
Sulfitionen haben die kürzeren #"S-O"# Fesseln.
Erläuterung:
Die Lewis-Struktur von #"SO"_3# is

(Ab chemistry.stackexchange.com)
Es hat insgesamt sechs σ- und π-Bindungen zu den drei #"O"# Atome.
Die durchschnittliche Anleiheordnung von a #"S-O"# Bindung ist #6/3=2#.
Die Lewis-Struktur von #"SO"_3^(2-)# is
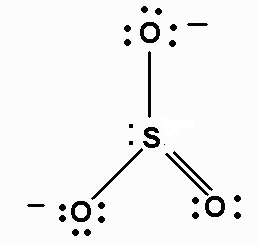
Es ist ein Resonanzhybrid mit insgesamt vier σ- und π-Bindungen zu den drei #"O"# Atome.
Die durchschnittliche Anleiheordnung von a #"S-O"# Bindung ist #4/3≈1.33#.
Da die Bindungslänge mit zunehmender Bindungsordnung abnimmt, #"SO"_3# wird vorausgesagt, dass die Bindungslänge kürzer ist.

(Ab en.wikipedia.org)

