Kann jemand s-, p-, d- und f-Orbitale in Bezug auf Größe, Form und Energie vergleichen?
Antworten:
Das ist eine schöne Frage - einfach zu stellen, schwer zu beantworten. Ich werde es versuchen....
Erläuterung:
Wir müssen einige Parameter für diese Frage einstellen. offensichtlich existieren s, p, d und f alle auf verschiedenen Quantenniveaus.
Nehmen wir jedoch das Quantenniveau n = 4 (das erste Quantenniveau, auf dem alle 4-Unterschalen - s, p, d, f - existieren), dann könnten Sie anfangen, einige Vergleiche anzustellen.
Man könnte zum Beispiel einfach die Modelle und sagen, dass alle 4-Unterschalen ungefähr den gleichen Durchmesser haben - das heißt, dass sie alle ähnliche Abstände vom Atomkern zum Hauptbereich des Elektrons haben Dichte (oder Volumen der größten Wolkenwahrscheinlichkeit).
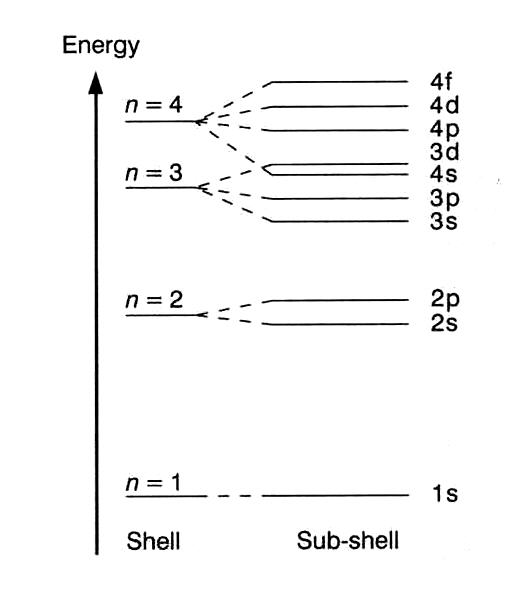
Die Energie jeder Unterschale ist jedoch sehr unterschiedlich - die 4s sind also wesentlich stabiler als die 4f - weshalb Atome die 4s-Unterschale vor der 4f füllen. Dies führt natürlich zu dem Quantenpegel-Aufteilungsdiagramm, mit dem Sie möglicherweise vertraut sind:
 )
)
Die Formen können nicht verglichen werden, da sie alle einzigartig sind. Sie können alle s-Orbitale vergleichen - da diese alle die gleiche Form (sphärisch) haben, ebenso alle p-Orbitale (Hantel) usw. Der einzige Unterschied ist die Größe - also ist 1 eine kleine Kugel, 2 eine größere Kugel , 3s noch größere Kugel etc.
das könnte mehr helfen,
(http://hyperphysics.phy-astr.gsu.edu/hbase/Chemical/eleorb.html)

