Welche der folgenden Verbindungen hat die höchste Gitterenergie?
Antworten:
(1) MgO hat die höchste Gitterenergie.
Erläuterung:
Die Gitterenergie hängt von der Anziehung zwischen den entgegengesetzt geladenen Ionen ab.
Die Anziehungskraft #F# ist direkt proportional zu den Gebühren (#q_1# und #q_2#) auf die beiden Ionen und auf die Entfernung #r# zwischen ihnen.
#F = (q_1q_2)/r^2#
Der Abstand zwischen den Gebühren #r# ist die Summe der Ionenradien.
#r = r_"anion" + r_"cation"#
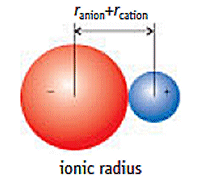
Die größte Anziehungskraft liegt also zwischen Ionen mit den kleinsten Radien.

Und da die Anziehungskraft vom Produkt der Ladungen abhängt, suchen wir nach Ionen mit der größten Ladung.
Sowohl in CaO als auch in MgO sind die Ladungen + 2 und -2, so dass die Wahl zwischen diesen beiden Oxiden besteht.
Die kleinsten Ionen können sich am nächsten kommen.
Sie haben den geringsten Abstand zwischen den Zentren und die größten Gitterenergien.
Die kleinsten Ionen befinden sich oben auf der Periodensystem.
#"Mg"^(2+)# ist kleiner als #"Ca"^(2+)#, damit #"MgO"# hat die größte Gitterenergie.

