Was sind s, p, d, f-Orbitale?
Antworten:
Orbitale sind die Regionen des Weltraums, in denen Elektronen am wahrscheinlichsten zu finden sind.
Erläuterung:
Jedes Orbital ist mit einer Zahl und einem Buchstaben gekennzeichnet.
Die Zahl gibt das Energieniveau des Elektrons im Orbital an. Somit bezieht sich 1 auf das Energieniveau, das dem Kern am nächsten liegt; 2 bezieht sich auf die nächste Energieebene weiter außen und so weiter.
Der Buchstabe bezieht sich auf die Form des Orbitals. Die Buchstaben sind in der Reihenfolge s, p, d, f, g, h, i, j usw. angeordnet. Die Buchstaben s, p, d und f wurden aus historischen Gründen vergeben, die uns nicht betreffen müssen. Wir müssen uns nur an die Formen erinnern, die den einzelnen Buchstaben entsprechen.
Da ein Elektron theoretisch den gesamten Raum einnehmen kann, ist es unmöglich, ein Orbital zu zeichnen. Wir können nur eine Form zeichnen, die die meiste Zeit das Elektron enthält, sagen wir 95% der Zeit. Wir nennen diese Form die 95% -Kontur.
s ORBITALE
Ein s-Orbital ist rund um den Atomkern kugelsymmetrisch wie eine hohle Kugel aus ziemlich flauschigem Material mit dem Kern im Zentrum. Wenn die Energieniveaus zunehmen, befinden sich die Elektronen weiter vom Kern entfernt, so dass die Orbitale größer werden. Die Größenordnung ist 1s <2s <3s <…, wie unten gezeigt.
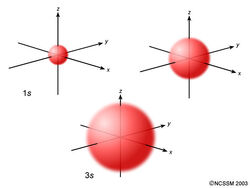
Betrachten wir nun einen Querschnitt dieser Orbitale.

Wenn Sie genau hinschauen, werden Sie feststellen, dass ein 1-Orbital sehr wenig Elektronen enthält Dichte in der Nähe des Kerns, aber es baut sich bis zu einem Maximum auf, wenn Sie weiter vom Kern entfernt sind, und nimmt dann über die Kontur hinaus ab. Es ist wie ein hohler Tennisball.
Ein 2s-Orbital ähnelt einem 1s-Orbital, hat jedoch eine Elektronendichtekugel in der äußeren Kugel, wie ein Tennisball in einem anderen. Zwischen den beiden Kugeln befindet sich eine Oberfläche, auf der mit null Wahrscheinlichkeit ein Elektron gefunden werden kann. Wir nennen diese Fläche einen Knoten oder eine Knotenfläche.
Ein 3s-Orbital ist noch größer und hat drei Knoten.
p ORBITALE
Nicht alle Elektronen bevölkern die Orbitale. Auf der ersten Energieebene ist das einzige Orbital, das Elektronen zur Verfügung steht, das 1-Orbital. Auf der zweiten Ebene gibt es jedoch zusätzlich zum 2s-Orbital auch Orbitale, die als 2p-Orbitale bezeichnet werden.
Im Gegensatz zu einem S-Orbital zeigt ein P-Orbital in eine bestimmte Richtung. Die unten gezeigte zeigt auf und ab der Seite.

Bei jedem Energieniveau gibt es drei absolut äquivalente p-Orbitale, die rechtwinklig zueinander ausgerichtet sind. Diese erhalten willkürlich die Symbole px, py und pz. Dies dient lediglich der Bequemlichkeit, da sich das, was Sie als x-, y- oder z-Richtung betrachten, ständig ändert, wenn das Atom im Raum fällt.
Die p-Orbitale auf der zweiten Energieebene heißen 2px, 2py und 2pz. Es gibt ähnliche Orbitale auf folgenden Ebenen: 3px, 3py, 3pz, 4px, 4py, 4pz und so weiter.
Alle Ebenen außer der ersten haben p-Orbitale.

d ORBITALE
Zusätzlich zu den s- und p-Orbitalen gibt es zwei weitere Orbitalsätze, in denen Elektronen mit höheren Energieniveaus leben können. Auf der dritten Ebene gibt es einen Satz von fünf d-Orbitalen (mit komplizierten Formen und Namen) sowie die 3- und 3p-Orbitale (3px, 3py, 3pz). Auf der dritten Ebene gibt es insgesamt neun Orbitale.
Die fünf 3d-Orbitale werden aufgerufen
3dxy
3dxz
3dyz
3dx² - y²
3dz²

Um die Namen zu verstehen, müssen wir sie in zwei Gruppen betrachten. Die erste Gruppe enthält die Orbitale 3dxy, 3dxz und 3dyz. Die Namen besagen, dass diese Orbitale in der xy-Ebene, der xz-Ebene und der yz-Ebene liegen. Jedes Orbital hat vier Lappen, und jeder der Lappen zeigt zwischen zwei der Achsen, nicht entlang dieser.
Die zweite Gruppe enthält die Orbitale 3dx² - y² und 3dz². Ihre Lappen zeigen entlang der verschiedenen Achsen.
Das 3dx² - y²-Orbital sieht genauso aus wie die erste Gruppe, außer dass die Lappen entlang der x- und y-Achse und nicht zwischen ihnen zeigen.
Der 3dz² sieht aus wie ein Orbital, das einen Donut um die Taille trägt.
f ORBITALE
Ab der vierten Ebene gibt es zusätzlich zu den 4-, 4p- und 4d-Orbitalen sieben weitere Orbitale.
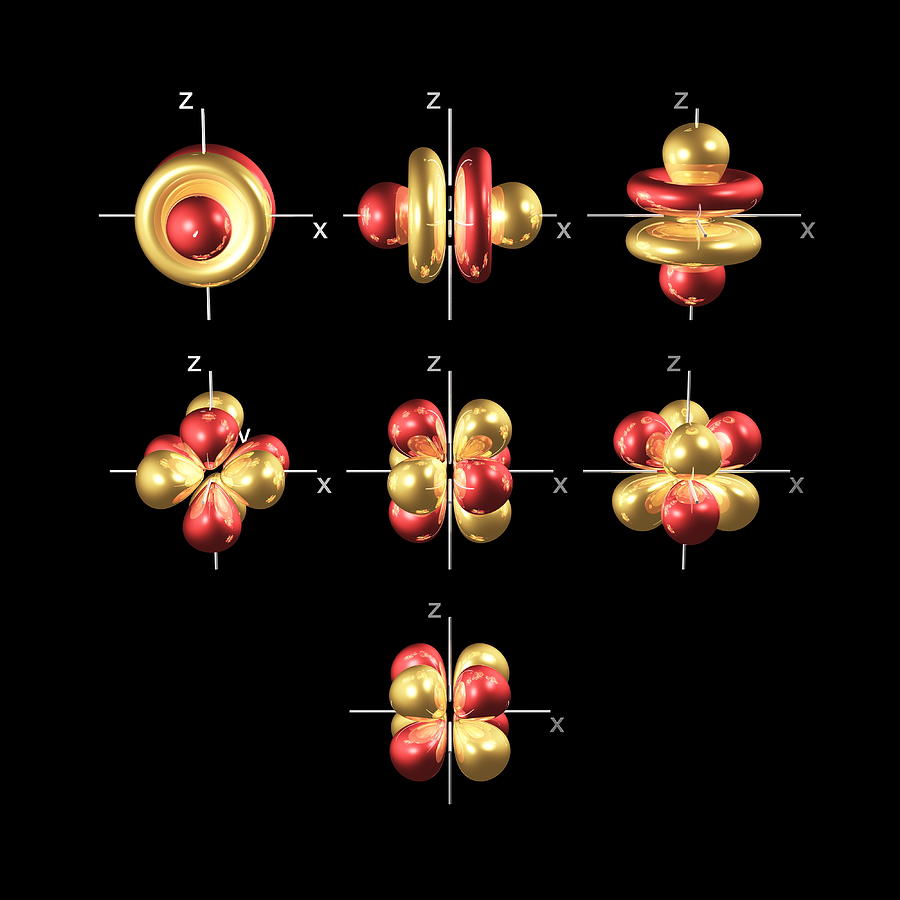
Zählt man die 4-, 4p- und 4d-Orbitale, ergibt dies insgesamt 16-Orbitale in der vierten Ebene. Sie haben noch kompliziertere Formen. s-, p-, d- und f-Orbitale sind auch bei allen höheren Energieniveaus verfügbar. Glücklicherweise müssen Sie sich die Formen der F orbitale wahrscheinlich nicht merken. Denken Sie daran, dass es in jedem Level ab Level 4 sieben F-Orbitale gibt.

