Was sind Metallaktivitätsreihen?
Eine Aktivitätsreihe ist eine Liste von Substanzen, die nach ihrer relativen Reaktivität geordnet sind.
Beispielsweise kann Magnesiummetall Wasserstoffionen aus der Lösung verdrängen. Magnesium ist also reaktiver als Wasserstoff:
Mg (s) + 2H⁺ (aq) → H₂ (g) + Mg²⁺ (aq)
Zinkmetall kann auch Wasserstoffionen aus der Lösung verdrängen:
Zn (s) + 2H⁺ (aq) → H₂ (g) + Zn²⁺ (aq)
Zink ist also auch aktiver als Wasserstoff.
Aber Magnesiummetall kann Zinkionen aus der Lösung verdrängen:
Mg (s) + Zn² & spplus; (aq) → Zn (s) + Mg² & spplus; (aq)
Magnesium ist also aktiver als Zink.
Die Aktivitätsreihe einschließlich dieser Elemente wäre Mg> Zn> H.
In ähnlicher Weise haben Chemiker eine komplette Aktivitätsreihe aufgebaut.
Die aktivsten Metalle stehen ganz oben auf der Tabelle. die am wenigsten aktiven sind unten.
Jedes Metall, das in der Reihe höher ist, verdrängt ein Metall, das sich darunter befindet, in einer einzigen Verdrängungsreaktion.
In der Sprache der Elektrochemie reduziert jedes Metall die Ionen der Metalle, die in der Reihe darunter liegen.
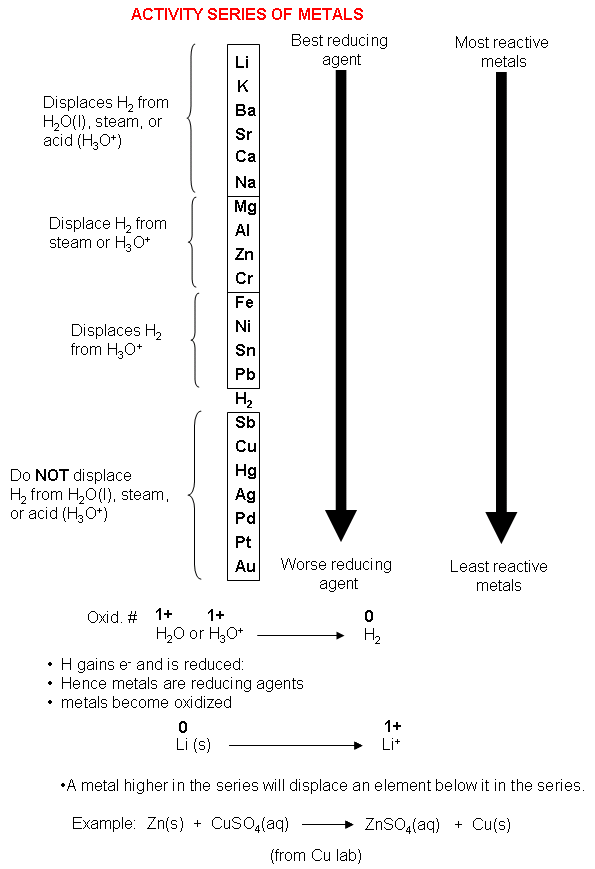
Das folgende Video zeigt ein Experiment zum Vergleich der Aktivität von drei Metallen. Zink, Kupfer und Magnesium.

