Was ist die Bindungspolarität von CH4?
Antworten:
Der Dipolmoment von a #"C-H"# Anleihe ist wahrscheinlich 0.34 D.
Erläuterung:
Wir sagen oft, dass a #"C-H"# Bindung ist unpolar, weil die Elektronegativitäten von #"C"# und #"H"# sind so nah beieinander.
Die Werte sind jedoch #"C = 2.55"# und #"H = 2.20"#.
Die Differenz entspricht 3% ionischem Charakter, also a #"C-H"# Die Bindung sollte einen kleinen Dipolmoment haben.
Aus experimentellen IR-Intensitäten von Methan können wir schließen, dass #µ_text(C-H) = "0.34 D"#, gerichtet #stackrelcolor(blue)(δ⁻)("C")"-"stackrelcolor(blue)(δ⁺)("H")#.
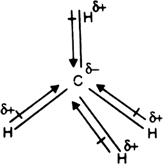
Theoretische Berechnungen ergeben unterschiedliche Ergebnisse, aber die meisten experimentellen Werte liegen zwischen 0.3 D und 0.4 D.

