Warum wird bei Grignard-Reaktionen Ether als Lösungsmittel verwendet?
Antworten:
Ether wird als Lösungsmittel verwendet, da es aprotisch ist und das Magnesiumion solvatisieren kann.
Erläuterung:
Eine Grignard-Reaktion beinhaltet die Reaktion eines Alkyl- (oder Arylhalogenids) mit Magnesiummetall unter Bildung eines Alkylmagnesiumhalogenids.
#"R-X" + "Mg" stackrelcolor(blue)("dry ether"color(white)(X))(→) "R-MgX"#
Diethylether ist aus zwei Gründen ein besonders gutes Lösungsmittel für die Bildung von Grignard-Reagenzien.
(a) Ether ist ein aprotisches Lösungsmittel
Die #"R-Mg"# Bindung ist hochpolar: #stackrelcolor(blue)(δ^(-))("R"color(white)(l))-stackrelcolor (blue)(δ^+)("Mg")"X"#
Der Grignard-Kohlenstoff ist stark basisch und reagiert mit den sauren Protonen polarer Lösungsmittel wie Wasser zu einem Alkan.
#stackrelcolor (blue)(δ^(-))("R"color(white)(l))"-"stackrelcolor (blue)(δ^+)("Mg")"X" + "H-OH" → "R-H" + "HO-MgX"#
Ether hat keine sauren Protonen, daher sind Grignard-Reagenzien in Ether stabil.
(b) Ether ist ein hervorragendes Solvatisierungsmittel
Die #"MgX"# Bindung in einem Grignard-Reagenz ist ionisch: #"R-Mg"^+ color(white)(l)"X"^-#.
Daher ist es schwierig, ein Grignard-Reagens in einem unpolaren Lösungsmittel zu bilden.
Die #"C-O"# Die Bindung in einem Äther ist ziemlich polar, und der Sauerstoff des Dipols kann sich solvatisieren und stabilisieren #"R-Mg"^+# Ion.
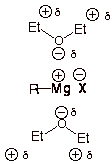
Somit sind Grignard-Reagenzien in Ether löslich.

